
EBV(又称人类疱疹病毒4型)是第一个被发现与人类肿瘤有关的DNA病毒。据估计,EBV相关肿瘤每年新发病例约20万例,每年死亡病例约占全部恶性肿瘤死亡病例的1.8%【1】。EBV可导致多种细胞来源的肿瘤,包括B细胞来源的Burkitt淋巴瘤、经典霍奇金淋巴瘤、B细胞淋巴瘤等,NK/T细胞来源的鼻型NK/T细胞淋巴瘤,上皮细胞来源的鼻咽癌、胃腺癌以及间叶细胞来源的平滑肌肉瘤。其中,EBV相关上皮细胞来源肿瘤占全部EBV相关恶性肿瘤的80%,鼻咽癌(NPC)组织中EBV的DNA检出率在90%以上[2,3]。因此,EBV相关蛋白作为NPC免疫治疗的靶点,受到广泛关注。
1. EBV潜伏感染
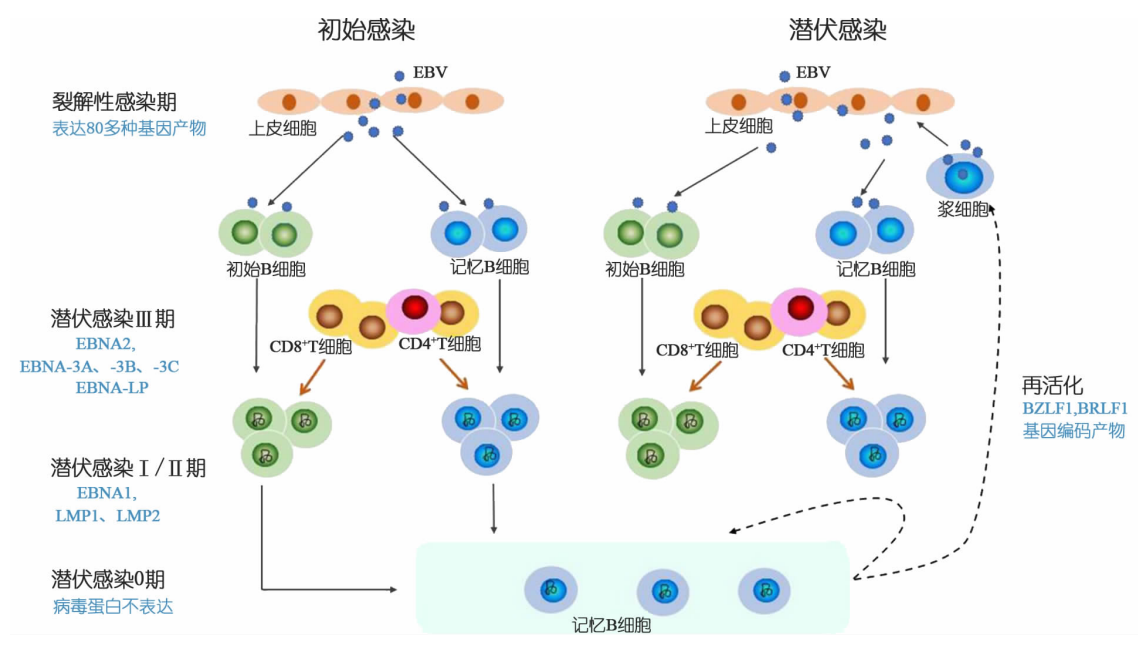
EBV感染周期包括初始感染和潜伏感染。EBV主要通过唾液接触传播,首先感染上皮细胞和B细胞,形成初始感染,继而在B细胞内形成潜伏感染。在宿主的免疫力底下或环境改变等情况下,EBV会被大量激活,进入裂解复制阶段,引发疾病[4]。
2. EBV免疫治疗关键蛋白
EB病毒在潜伏感染时11个基因表达产物,包括6种核抗原(EBNA1、EBNA2、EBNA3A、EBNA3B、EBNA3C和EBNA-LP)、3种潜伏膜蛋白(LMP1、LMP2A、LMP2B)及2种小核糖核酸(EBER1、EBER2)。根据EBV编码蛋白的表达情况不同,潜伏感染可分为:①潜伏Ⅰ型 表达EBNA1、EBERs,见于伯基特淋巴瘤;②潜伏Ⅱ型 表达EBNA1、LMP1、LMP2、EBERs,常见于鼻咽癌、霍奇金淋巴瘤等恶性肿瘤;③潜伏Ⅲ型,表达所有六种核抗原、LMP1、LMP2以及EBERs,是免疫母细胞性淋巴瘤以及艾滋病相关淋巴瘤常见的感染类型[5,6]。
此外,EBV基因组具有高度的变异性,不同的变异体致病力不同。研究发现,EBV基因组中发生变异主要是编码LMP1、EBNA2和EBNA3蛋白家族的基因;其次是BDLF3(编码蛋白gp150)、BLLF1(编码gp350/200)、BNLF2a(与免疫逃逸有关)、BZLF1、BRRF2等基因[7]。
3. EBV MHC-1 Tetramer助力鼻咽癌免疫治疗研发
CD8+T细胞上表达的T细胞受体(TCR)可以特异性识别MHC-抗原肽复合物,并与其结合,进而直接攻击并杀伤病原感染细胞、癌细胞等靶细胞。基于上述原理, Altman 等(1996年)使用MHC-抗原肽复合物形成的四聚体试剂,成功地利用流式细胞仪在单个细胞水平上对特异性T 细胞进行了检测。与传统的通过检测细胞因子、细胞毒性活性等间接检测方式不同,该技术不仅可以直接检测和分离抗原特异性T 细胞,也可以实现对其功能与表型等的详细分析,成为CTL细胞免疫应答监测的金标准,可在肿瘤免疫治疗领域广泛应用。
广州好芝生物科技有限公司研发团队结合EBV致癌研究热点抗原表位肽最新成果,采用最新的抗原表位肽预测算法,结合中国人群高频HLA-A*0201/1101/2402,设计生产了相应的EBV MHC-I Tetramer,旨在助力EBV疫苗、TCR-T等免疫治疗产品研发及治疗后临床疗效评估。
抗原 | 序列 | MHC | Location |
BMLF1 | GLCTLVAML | HLA-A*0201 | 259~267 |
BMLF1 | TLDYKPLSV | HLA-A*0201 | 208~216 |
BRLF1 | YVLDHLIVV | HLA-A*0201 | 109~117 |
EBNA3A | RYSIFFDY | HLA-A*2402 | 246~253 |
EBNA3B | TYSAGIVQI | HLA-A*2402 | 217~225 |
EBNA3B | IVTDFSVIK | HLA-A*1101 | 416~424 |
EBNA3B | AVFDRKSDAK | HLA-A*1101 | 399~408 |
LMP1 | YLLEILWRL | HLA-A*0201 | 125~133 |
LMP1 | YLQQNWWTL | HLA-A*0201 | 159~167 |
LMP2 | KILLARLFLY | HLA-A*1101 | 349~358 |
LMP2 | SSCSSCPLSKI | HLA-A*1101 | 340~350 |
LMP2 | LLWTLVVL | HLA-A*0201 | 329~336 |
LMP2 | TVCGGIMFL | HLA-A*0201 | 243~251 |
LMP2 | FLYALALLL | HLA-A*0201 | 356~364 |
LMP2 | CLGGLLTMV | HLA-A*0201 | 426~434 |
LMP2 | PYLFWLAAI | HLA-A*2402 | 131~139 |
LMP2 | TYGPVFMCL | HLA-A*2402 | 419~427 |
BZLF1 | SQAPLPCVL | HLA-E*01033 | 40~48 |
参考文献:
[1] Khan G., Hashim M.J., Global burden of deaths from EpsteinBarr virus attributable malignancies 1990-2010.Infect Agent Cancer,2014,9( 1) : 38
[2] Cohen J.I., Fauci A.S., Varmus H., Nabel G.J. Epstein-Barr Virus: an important vaccine target for cancer prevention. Sci Transl Med,2011, 3: 107
[3] Tsao S..W., Tsang C.M., To K.F., & Lo K.W. The role of Epstein-Barr virus in epithelial malignancies. J Pathol 235(2): 323-333
[4] 刘璐瑶等. EB病毒感染的免疫机制研究进展, 中国循证儿科杂质, 2017, 12(3): 219-232
[5] Grywalska E., Markowicz J., Grabarczyk P. Epstein-Barr virus-associated lymphoproliferative disorders. Postepy higieny i medycyny doswiadczalnej 2013, 67: 481-490
[6] Asano N., Kato S., Nakamura S. Epstein-Barr virus-associated natural killer/T-cell lymphomas. Best practice & research Clinical haematology 2013, 26(1):15-21
[7] Palser A.L., Grayson N.E., White R.E., et al. Genome diversity of Epstein-Barr virus from multiple tumor type and normal infection. J Virol, 2015, 89(10): 5222-5237